مدل سازی الکتروآنالیز: ولتامتری چرخه ای
اگر شما یک الکتروشیمیدان نیستید، به احتمال زیاد هرگز با ولتامتری حلقوی برخورد نکرده اید. اما به هر مجله الکتروشیمیایی، مقالات کنفرانس یا وب سایت شرکت تولید کنندگان حسگرهای الکتروشیمیایی نگاه کنید. در جایی نزدیک به جلو، نمودار متمایز “دو قله” را خواهید دید.
چرا ولتامتری چرخه ای انجام دهیم؟
نمودار “دو قله” به صورت زیر است:
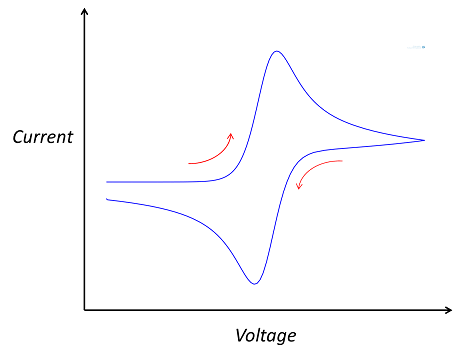
این یک ولتاموگرافی حلقوی است که در آن جریان (“آمتری”) در برابر ولتاژ اعمال شده به یک سلول الکتروشیمیایی رسم می شود. ولتاژ در طیفی از مقادیر بالا و پایین می رود تا به طور متوالی در جهت مخالف یک واکنش الکترولیز حرکت کند:
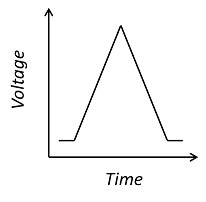
ولتامتری چرخه ای یک تکنیک بسیار مورد استفاده برای بررسی فیزیک و شیمی در سطح مشترک بین الکترود و الکترولیت، مانند محلول نمکی است. سطوح الکترواکتیو برای همه دستگاههای الکتروشیمیایی، از جمله دستگاههای استخراج انرژی رایج مانند باتریها و سلولهای سوختی، و همچنین حسگرهای الکتروشیمیایی، مانند آنهایی که افراد دیابتی برای نظارت بر غلظت گلوکز خون استفاده میکنند، مشترک است. علاوه بر این، شیمی رابط الکترود-الکترولیت هنوز به طور کامل درک نشده است و یک زمینه فعال تحقیقات دانشگاهی است.
ولتامتری می تواند برای تأیید و طراحی دستگاه ارزشمند باشد زیرا یک اسکن واحد حاوی اطلاعات زیادی در مورد رفتار شیمیایی و فیزیکی یک سیستم است. همچنین، ولتامتری میتواند حالت اساسی عملکرد یک حسگر باشد، زیرا جریان اندازهگیری شده به طور خطی به غلظت آنالیت در یک سیستم خوب طراحی شده وابسته است. اصلاح شیمیایی مواد الکترود میتواند ولتامتری را برای ترکیبات بیولوژیکی یا گازهای سمی در یک مخلوط خاص کند، و این یک تکنیک ارزان است که در آن پیشرفتهایی مانند الکترودهای چاپ شده با صفحه نمایش «الکتروشیمی یکبار مصرف» را امکانپذیر میسازد.
برای طراحی و تحقیق، مزیت بزرگ ولتامتری، تنوع اطلاعاتی است که ارائه می دهد. این رقابت بین سرعت الکترولیز در سطح الکترود و سرعت انتقال گونههای شیمیایی واکنشدهنده به آن سطح توسط انتشار را نشان میدهد و همچنین میتواند اطلاعات ارزشمندی از مکانیسم و سرعت واکنشهای شیمیایی در محلول به دست دهد. با انجام ولتامتری در نرخهای مختلف اسکن، که در آن نرخ تغییر ولتاژ در زمان تغییر میکند، میتوان مقیاسهای زمانی مختلف سیستم و بنابراین پدیدههای فیزیکی متفاوت را مشاهده کرد.
چرا مدل ولتامتری؟
با همه اهمیتی که دارد، ولتامتری یک تکنیک دشوار برای درک است. تمام اثرات فیزیکی واقعی در سیستم به منحنی های نسبتاً محرمانه جریان-ولتاژ تبدیل می شوند. اگرچه ممکن است شیمیدانان باتجربه الکتروتحلیلی بتوانند به طور شهودی شیمی را در یک ولتاموگرام “دیدن” کنند، برای به دست آوردن اطلاعات کمی از آزمایش ها، مقایسه ولتامتری با یک پیش بینی نظری ضروری است. از آنجایی که سینتیک های الکتروشیمیایی اغلب غیرخطی هستند و ولتامتری یک مسئله گذرا است، این نظریه برای حل های تحلیلی قابل قبول نیست، مگر در موارد محدودی، و بنابراین شبیه سازی کامپیوتری ضروری است.
ساده نگه داشتن مدل
ماژول الکتروشیمی جدید COMSOL شامل یک الکتروآنالیز استرابط مناسب برای مدلسازی تکنیکهای الکتروتحلیلی مانند ولتامتری. این رابط حضور مقدار زیادی الکترولیت پشتیبان را فرض می کند. نمک بی اثر، مانند کلرید پتاسیم، که به طور مصنوعی به الکترولیت در سلول الکتروشیمیایی اضافه می شود تا رسانایی آن را افزایش دهد. پشتیبانی از الکترولیت میدان های الکتریکی را کاهش می دهد، که سودمند است زیرا هم تحلیل تجربی و هم تئوری اساسی را ساده می کند. ما فرض میکنیم که تنها انتشار به انتقال گونههای شیمیایی کمک میکند، زیرا محلول به هم نخورده است و بازههای زمانی به اندازهای کوتاه هستند که همرفت طبیعی در محلول مهم نیست. در این شرایط، معادلات حمل و نقل گونه های شیمیایی خطی هستند و حل آنها بسیار آسان تر است.
مقیاس های طول انتشار در طول مدت معمول آزمایش ولتامتری بسیار کوتاه هستند – اغلب بسیار کمتر از 1 میلی متر. برای یک “ماکروالکترود” سنتی، به شکل دیسکی با شعاع بیش از 1 میلی متر، این درست است که فرض کنیم که انتشار فقط در جهت عادی به سطح الکترود قابل توجه است و می توان از تاثیر لبه الکترود چشم پوشی کرد. بنابراین واکنش ها و انتقال در سراسر سطح الکترود یکنواخت است. این امر آنالیز ولتامتری را به یک مسئله وابسته به زمان یک بعدی تبدیل می کند.
راه اندازی مدل ولتامتری چرخه ای
برای تسهیل تعریف ولتاژ اعمال شده گذرا و تأثیر آن بر سرعت واکنش الکترولیز، رابط الکتروآنالیز حاوی یک ویژگی از پیش ساخته شده “سطح الکترود” است که اجازه می دهد تا پنجره پتانسیل و نرخ اسکن ولتاموگرافی مستقیماً تنظیم شود. این ویژگی همچنین به طور خودکار معادله باتلر-ولمر را برای سینتیک الکترود پیادهسازی میکند، اما، مانند هر ویژگی در COMSOL Multiphysics، یک عبارت تعریفشده توسط کاربر برای این سینتیکها میتواند جایگزین شود. مطالعه ولتامتری چرخه ای مرتبط سپس به طور خودکار مسئله وابسته به زمان مربوطه را با استفاده از روش های عددی مناسب برای ادغام معادله انتشار وابسته به زمان حل می کند . طیف وسیعی از نرخ های اسکن را می توان در یک محاسبات با استفاده از ویژگی “Sweep پارامتریک” مطالعه کرد.
نگاهی به نتایج
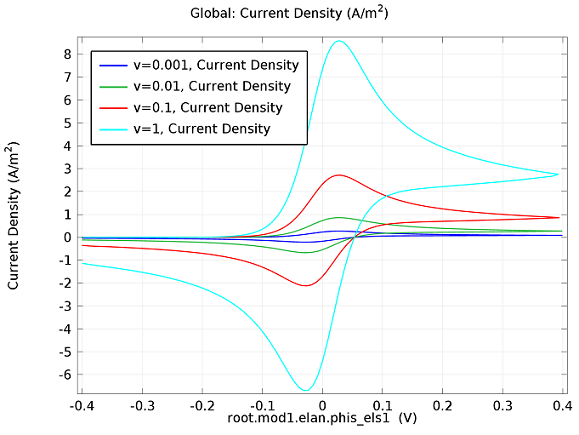
در شکل بالا، چهار ولتاموگرام پیشبینیشده را میبینیم که با چهار سرعت اسکن متوالی، از 1 میلیولت بر ثانیه تا 1 ولت بر ثانیه ثبت شدهاند. اینها با مدت زمان آزمایشی از تقریباً نیم ساعت تا کمی بیش از یک ثانیه مطابقت دارند. مشاهده میشود که جریانها با سرعت اسکن افزایش مییابند، اما ولتاموگرافیها همان ظاهر کیفی «دو قله» را دارند. مورد دوم را می توان توضیح داد زیرا، برای شروع، ولتاژ در محدوده ای است که واکنش رو به جلو واکنش دهنده رانده نمی شود، بنابراین جریان ناچیزی وجود دارد. همانطور که ولتاژ بالا می رود، واکنش تسریع می شود، بنابراین جریان افزایش می یابد. با این حال، پس از مدتی، غلظت واکنش دهنده توسط واکنش در سطح الکترود کاهش می یابد. سپس فرآیند تعیین نرخ تغییر می کند، به طوری که جریان با انتشار واکنش دهنده به سطح کنترل می شود. و در نتیجه دوباره سقوط می کند. یک فرآیند مشابه به صورت معکوس برای واکنش برگشتی رخ می دهد که در آن محصول دوباره به واکنش دهنده اصلی تبدیل می شود زیرا ولتاژ به نقطه شروع خود اسکن می شود.
افزایش چگالی جریان با سرعت اسکن به این دلیل اتفاق میافتد که اسکن سریعتر باعث میشود لایه انتشار در فاصله کوتاهتری ایجاد شود. از آنجایی که غلظت از توده تا صفر در طول باریکتر تغییر میکند، شار انتشاری بزرگتر است، بنابراین جریان نیز همینطور است. جریان اوج در واقع باید با ریشه مربع سرعت اسکن مقیاس شود: بررسی این رابطه یک روش تأیید متداول برای دادههای تجربی است تا بررسی شود که اندازهگیری توسط اثرات فیزیکی به غیر از انتشار خراب نشده است.
برای طراحی حسگر، ما همیشه می خواهیم جریان خود را به حداکثر برسانیم تا حساسیت را به حداکثر برسانیم، بنابراین این تحلیل می تواند در طراحی عملی سلول الکتروشیمیایی و محیط شیمیایی کمک کند. مقایسه ولتاموگرامهای پیشبینیشده و اندازهگیری شده، تعیین خواص مواد و سایر پارامترهای سیستم را که ممکن است ناشناخته باشند، مانند ضرایب انتشار و سرعت واکنش، امکانپذیر میسازد.
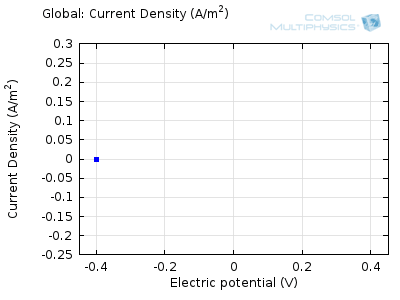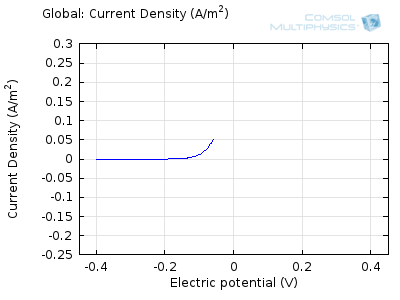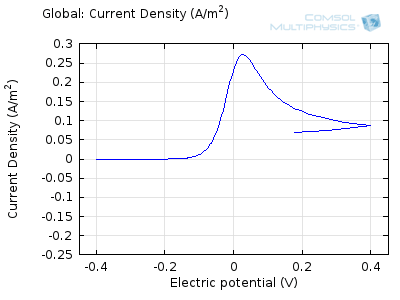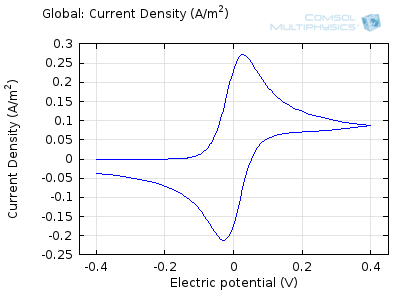
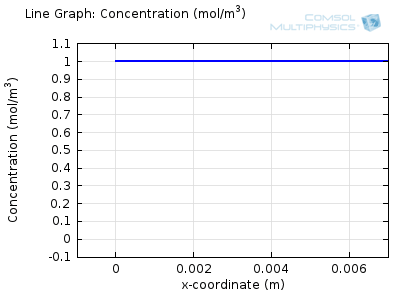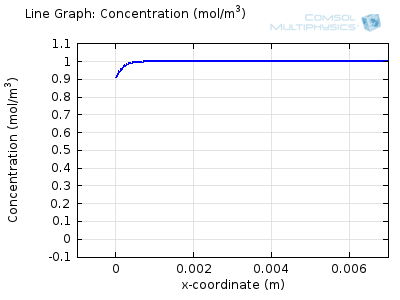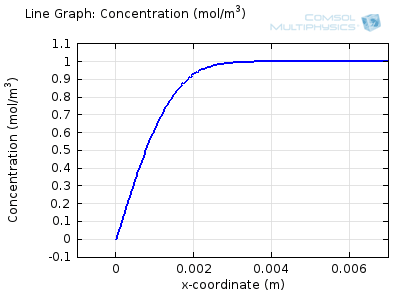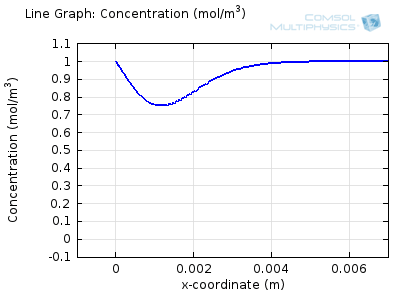
سعی کنید انیمیشن های فوق را با هم مقایسه کنید تا رابطه بین نمایه غلظت فعلی و در حال تکامل را درک کنید. توجه داشته باشید که چگونه غلظت در سطح الکترود (x = 0) با افزایش جریان به صفر می رسد، سپس، هنگامی که غلظت سطح صفر شد، گرادیان غلظت تحت نفوذ شل می شود و جریان نیز شل می شود. با معکوس شدن جریان توسط واکنش معکوس در طول بخش دوم جارو، غلظت به مقدار عمده خود در سطح الکترود باز می گردد.
رفتن به جلو
از آنجایی که رابط Electroanalysis مدل سازی الکتروتحلیلی را در محیط COMSOL Multiphysics تعبیه می کند، یک رابط کاربری قدرتمند و منعطف برای روش های اجزای محدود، به طور مستقیم امکان گسترش دامنه این مدل وجود دارد. واکنشهای شیمیایی بعدی گونههای تولید شده بهصورت الکتروشیمیایی را میتوان با افزودن یک شرط دامنه واکنشها گنجاند. یک مدل دو بعدی یا سه بعدی از همان فرآیند را می توان برای مطالعه انتشار در یک هندسه سیستم واقعی تنظیم کرد. چرخه های ولتامتری چندگانه را می توان انجام داد، یا می توان از شکل موج های ولتاژ غیر استاندارد استفاده کرد. جفت شدن به یک محاسبه جریان سیال با همرفت گونه های واکنش دهنده امکان بررسی الکتروشیمی هیدرودینامیکی را فراهم می کند. ما همچنین میتوانیم طیف وسیعی از تکنیکهای مرتبط مانند کرونوآمپرومتری پلهای پتانسیل و طیفسنجی امپدانس الکتروشیمیایی را از طریق رابط کاربری مشابه در نظر بگیریم.
نکته: ولتامتری چرخه ای را در یک مدل الکترود در گالری مدل بررسی کنید .
اگر شما یک الکتروشیمیدان نیستید، به احتمال زیاد هرگز با ولتامتری حلقوی برخورد نکرده اید. اما به هر مجله الکتروشیمیایی، مقالات کنفرانس یا وب سایت شرکت تولید کنندگان حسگرهای الکتروشیمیایی نگاه کنید. در جایی نزدیک به جلو، نمودار متمایز “دو قله” را خواهید دید.
چرا ولتامتری چرخه ای انجام دهیم؟
نمودار “دو قله” به صورت زیر است:

این یک ولتاموگرافی حلقوی است که در آن جریان (“آمتری”) در برابر ولتاژ اعمال شده به یک سلول الکتروشیمیایی رسم می شود. ولتاژ در طیفی از مقادیر بالا و پایین می رود تا به طور متوالی در جهت مخالف یک واکنش الکترولیز حرکت کند:

ولتامتری چرخه ای یک تکنیک بسیار مورد استفاده برای بررسی فیزیک و شیمی در سطح مشترک بین الکترود و الکترولیت، مانند محلول نمکی است. سطوح الکترواکتیو برای همه دستگاههای الکتروشیمیایی، از جمله دستگاههای استخراج انرژی رایج مانند باتریها و سلولهای سوختی، و همچنین حسگرهای الکتروشیمیایی، مانند آنهایی که افراد دیابتی برای نظارت بر غلظت گلوکز خون استفاده میکنند، مشترک است. علاوه بر این، شیمی رابط الکترود-الکترولیت هنوز به طور کامل درک نشده است و یک زمینه فعال تحقیقات دانشگاهی است.
ولتامتری می تواند برای تأیید و طراحی دستگاه ارزشمند باشد زیرا یک اسکن واحد حاوی اطلاعات زیادی در مورد رفتار شیمیایی و فیزیکی یک سیستم است. همچنین، ولتامتری میتواند حالت اساسی عملکرد یک حسگر باشد، زیرا جریان اندازهگیری شده به طور خطی به غلظت آنالیت در یک سیستم خوب طراحی شده وابسته است. اصلاح شیمیایی مواد الکترود میتواند ولتامتری را برای ترکیبات بیولوژیکی یا گازهای سمی در یک مخلوط خاص کند، و این یک تکنیک ارزان است که در آن پیشرفتهایی مانند الکترودهای چاپ شده با صفحه نمایش «الکتروشیمی یکبار مصرف» را امکانپذیر میسازد.
برای طراحی و تحقیق، مزیت بزرگ ولتامتری، تنوع اطلاعاتی است که ارائه می دهد. این رقابت بین سرعت الکترولیز در سطح الکترود و سرعت انتقال گونههای شیمیایی واکنشدهنده به آن سطح توسط انتشار را نشان میدهد و همچنین میتواند اطلاعات ارزشمندی از مکانیسم و سرعت واکنشهای شیمیایی در محلول به دست دهد. با انجام ولتامتری در نرخهای مختلف اسکن، که در آن نرخ تغییر ولتاژ در زمان تغییر میکند، میتوان مقیاسهای زمانی مختلف سیستم و بنابراین پدیدههای فیزیکی متفاوت را مشاهده کرد.
چرا مدل ولتامتری؟
با همه اهمیتی که دارد، ولتامتری یک تکنیک دشوار برای درک است. تمام اثرات فیزیکی واقعی در سیستم به منحنی های نسبتاً محرمانه جریان-ولتاژ تبدیل می شوند. اگرچه ممکن است شیمیدانان باتجربه الکتروتحلیلی بتوانند به طور شهودی شیمی را در یک ولتاموگرام “دیدن” کنند، برای به دست آوردن اطلاعات کمی از آزمایش ها، مقایسه ولتامتری با یک پیش بینی نظری ضروری است. از آنجایی که سینتیک های الکتروشیمیایی اغلب غیرخطی هستند و ولتامتری یک مسئله گذرا است، این نظریه برای حل های تحلیلی قابل قبول نیست، مگر در موارد محدودی، و بنابراین شبیه سازی کامپیوتری ضروری است.
ساده نگه داشتن مدل
ماژول الکتروشیمی جدید COMSOL شامل یک الکتروآنالیز استرابط مناسب برای مدلسازی تکنیکهای الکتروتحلیلی مانند ولتامتری. این رابط حضور مقدار زیادی الکترولیت پشتیبان را فرض می کند. نمک بی اثر، مانند کلرید پتاسیم، که به طور مصنوعی به الکترولیت در سلول الکتروشیمیایی اضافه می شود تا رسانایی آن را افزایش دهد. پشتیبانی از الکترولیت میدان های الکتریکی را کاهش می دهد، که سودمند است زیرا هم تحلیل تجربی و هم تئوری اساسی را ساده می کند. ما فرض میکنیم که تنها انتشار به انتقال گونههای شیمیایی کمک میکند، زیرا محلول به هم نخورده است و بازههای زمانی به اندازهای کوتاه هستند که همرفت طبیعی در محلول مهم نیست. در این شرایط، معادلات حمل و نقل گونه های شیمیایی خطی هستند و حل آنها بسیار آسان تر است.
مقیاس های طول انتشار در طول مدت معمول آزمایش ولتامتری بسیار کوتاه هستند – اغلب بسیار کمتر از 1 میلی متر. برای یک “ماکروالکترود” سنتی، به شکل دیسکی با شعاع بیش از 1 میلی متر، این درست است که فرض کنیم که انتشار فقط در جهت عادی به سطح الکترود قابل توجه است و می توان از تاثیر لبه الکترود چشم پوشی کرد. بنابراین واکنش ها و انتقال در سراسر سطح الکترود یکنواخت است. این امر آنالیز ولتامتری را به یک مسئله وابسته به زمان یک بعدی تبدیل می کند.
راه اندازی مدل ولتامتری چرخه ای
برای تسهیل تعریف ولتاژ اعمال شده گذرا و تأثیر آن بر سرعت واکنش الکترولیز، رابط الکتروآنالیز حاوی یک ویژگی از پیش ساخته شده “سطح الکترود” است که اجازه می دهد تا پنجره پتانسیل و نرخ اسکن ولتاموگرافی مستقیماً تنظیم شود. این ویژگی همچنین به طور خودکار معادله باتلر-ولمر را برای سینتیک الکترود پیادهسازی میکند، اما، مانند هر ویژگی در COMSOL Multiphysics، یک عبارت تعریفشده توسط کاربر برای این سینتیکها میتواند جایگزین شود. مطالعه ولتامتری چرخه ای مرتبط سپس به طور خودکار مسئله وابسته به زمان مربوطه را با استفاده از روش های عددی مناسب برای ادغام معادله انتشار وابسته به زمان حل می کند . طیف وسیعی از نرخ های اسکن را می توان در یک محاسبات با استفاده از ویژگی “Sweep پارامتریک” مطالعه کرد.
نگاهی به نتایج

در شکل بالا، چهار ولتاموگرام پیشبینیشده را میبینیم که با چهار سرعت اسکن متوالی، از 1 میلیولت بر ثانیه تا 1 ولت بر ثانیه ثبت شدهاند. اینها با مدت زمان آزمایشی از تقریباً نیم ساعت تا کمی بیش از یک ثانیه مطابقت دارند. مشاهده میشود که جریانها با سرعت اسکن افزایش مییابند، اما ولتاموگرافیها همان ظاهر کیفی «دو قله» را دارند. مورد دوم را می توان توضیح داد زیرا، برای شروع، ولتاژ در محدوده ای است که واکنش رو به جلو واکنش دهنده رانده نمی شود، بنابراین جریان ناچیزی وجود دارد. همانطور که ولتاژ بالا می رود، واکنش تسریع می شود، بنابراین جریان افزایش می یابد. با این حال، پس از مدتی، غلظت واکنش دهنده توسط واکنش در سطح الکترود کاهش می یابد. سپس فرآیند تعیین نرخ تغییر می کند، به طوری که جریان با انتشار واکنش دهنده به سطح کنترل می شود. و در نتیجه دوباره سقوط می کند. یک فرآیند مشابه به صورت معکوس برای واکنش برگشتی رخ می دهد که در آن محصول دوباره به واکنش دهنده اصلی تبدیل می شود زیرا ولتاژ به نقطه شروع خود اسکن می شود.
افزایش چگالی جریان با سرعت اسکن به این دلیل اتفاق میافتد که اسکن سریعتر باعث میشود لایه انتشار در فاصله کوتاهتری ایجاد شود. از آنجایی که غلظت از توده تا صفر در طول باریکتر تغییر میکند، شار انتشاری بزرگتر است، بنابراین جریان نیز همینطور است. جریان اوج در واقع باید با ریشه مربع سرعت اسکن مقیاس شود: بررسی این رابطه یک روش تأیید متداول برای دادههای تجربی است تا بررسی شود که اندازهگیری توسط اثرات فیزیکی به غیر از انتشار خراب نشده است.
برای طراحی حسگر، ما همیشه می خواهیم جریان خود را به حداکثر برسانیم تا حساسیت را به حداکثر برسانیم، بنابراین این تحلیل می تواند در طراحی عملی سلول الکتروشیمیایی و محیط شیمیایی کمک کند. مقایسه ولتاموگرامهای پیشبینیشده و اندازهگیری شده، تعیین خواص مواد و سایر پارامترهای سیستم را که ممکن است ناشناخته باشند، مانند ضرایب انتشار و سرعت واکنش، امکانپذیر میسازد.


سعی کنید انیمیشن های فوق را با هم مقایسه کنید تا رابطه بین نمایه غلظت فعلی و در حال تکامل را درک کنید. توجه داشته باشید که چگونه غلظت در سطح الکترود (x = 0) با افزایش جریان به صفر می رسد، سپس، هنگامی که غلظت سطح صفر شد، گرادیان غلظت تحت نفوذ شل می شود و جریان نیز شل می شود. با معکوس شدن جریان توسط واکنش معکوس در طول بخش دوم جارو، غلظت به مقدار عمده خود در سطح الکترود باز می گردد.
رفتن به جلو
از آنجایی که رابط Electroanalysis مدل سازی الکتروتحلیلی را در محیط COMSOL Multiphysics تعبیه می کند، یک رابط کاربری قدرتمند و منعطف برای روش های اجزای محدود، به طور مستقیم امکان گسترش دامنه این مدل وجود دارد. واکنشهای شیمیایی بعدی گونههای تولید شده بهصورت الکتروشیمیایی را میتوان با افزودن یک شرط دامنه واکنشها گنجاند. یک مدل دو بعدی یا سه بعدی از همان فرآیند را می توان برای مطالعه انتشار در یک هندسه سیستم واقعی تنظیم کرد. چرخه های ولتامتری چندگانه را می توان انجام داد، یا می توان از شکل موج های ولتاژ غیر استاندارد استفاده کرد. جفت شدن به یک محاسبه جریان سیال با همرفت گونه های واکنش دهنده امکان بررسی الکتروشیمی هیدرودینامیکی را فراهم می کند. ما همچنین میتوانیم طیف وسیعی از تکنیکهای مرتبط مانند کرونوآمپرومتری پلهای پتانسیل و طیفسنجی امپدانس الکتروشیمیایی را از طریق رابط کاربری مشابه در نظر بگیریم.
نکته: ولتامتری چرخه ای را در یک مدل الکترود در گالری مدل بررسی کنید .
- لینک دانلود به صورت پارت های 1 گیگابایتی در فایل های ZIP ارائه شده است.
- در صورتی که به هر دلیل موفق به دانلود فایل مورد نظر نشدید به ما اطلاع دهید.
برای مشاهده لینک دانلود لطفا وارد حساب کاربری خود شوید!
وارد شویدپسورد فایل : پسورد ندارد گزارش خرابی لینک

دیدگاهتان را بنویسید