برای جریان آرام، یا زمانی که مدل واکنش آشفته در یک ویژگی روی هیچ تنظیم شده است (در حمل و نقل گونههای متمرکز)، نرخ واکنش پیشفرض (خودکار) که توسط ویژگی استفاده میشود بر اساس قانون عمل جرم است. یک واکنش کلی متعلق به مجموعه ای از واکنش های j و شامل گونه های i را در نظر بگیرید :
(6-94)
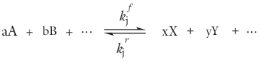
برای چنین مجموعه واکنشی، سرعت واکنش rj (واحد SI: mol/(m3 · s ))، را می توان با قانون عمل جرم توصیف کرد:
(6-95)
در اینجا،  و
و  به ترتیب ثابت نرخ رو به جلو و معکوس را مشخص کنید. غلظت گونه i را c i نشان می دهند (واحد SI: mol/m 3 ). ضرایب استوکیومتری ν ij نشان داده می شود و برای واکنش دهنده ها منفی و برای محصولات مثبت تعریف می شود. در عمل، یک واکنش به ندرت شامل برخورد بیش از دو گونه در یک مرحله واکنش می شود، به این معنی که یک بیان جنبشی معمولاً از درجه 2 یا کمتر است (با توجه به غلظت های درگیر).
به ترتیب ثابت نرخ رو به جلو و معکوس را مشخص کنید. غلظت گونه i را c i نشان می دهند (واحد SI: mol/m 3 ). ضرایب استوکیومتری ν ij نشان داده می شود و برای واکنش دهنده ها منفی و برای محصولات مثبت تعریف می شود. در عمل، یک واکنش به ندرت شامل برخورد بیش از دو گونه در یک مرحله واکنش می شود، به این معنی که یک بیان جنبشی معمولاً از درجه 2 یا کمتر است (با توجه به غلظت های درگیر).
علاوه بر وابستگی به غلظت، وابستگی دما را می توان با استفاده از عبارات از پیش تعریف شده آرنیوس برای ثابت های سرعت در نظر گرفت:
در اینجا، A ضریب فرکانس، n توان دما، E انرژی فعال سازی (واحد SI: J/mol) و Rg ثابت گاز، 8.314 J/(mol·K) را نشان می دهد. ضریب پیش نمایی، شامل ضریب فرکانس A و ضریب دما Tn ، واحدهای ( m3 /mol) α- 1 /s داده میشود ، که α ترتیب واکنش (با توجه به غلظتها) است.
.




