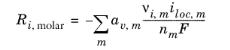برای تعریف ضرایب استوکیومتری، νi استفاده می شود ، که νi مثبت ( ν قرمز ) برای محصولات و منفی ( ν ox ) برای واکنش دهنده ها در واکنش احیا است . تعداد الکترون های شرکت کننده، n ، همیشه مثبت است.
شار گونه های مولی، Ni (واحد SI: mol/(m2 · s))، عمود بر سطح مشترک الکترود-الکترولیت با جمع کردن تمام مشارکت های شار از واکنش های الکترود شاخص m ، مطابق قوانین فارادی محاسبه می شود:
جایی که i loc، m چگالی جریان محلی (واحد SI: A/m 2 ) واکنش الکتروشیمیایی، n m تعداد الکترونهای شرکتکننده و F (واحد SI: C/mol) ثابت فارادی است . توجه داشته باشید که i loc، m نشان دهنده چگالی جریان عمود بر سطح الکترود است.