رابط باتری تک ذره، توزیع بار در باتری را با در نظر گرفتن انتشار جامد در ذرات الکترود و سینتیک واکنش میانافزایی مدلسازی میکند. افت پتانسیل اهمی در الکترولیت در مدل با استفاده از عبارت مقاومت محلول توده ای گنجانده شده است.
سلول E پتانسیل سلولی (واحد SI: V) به صورت تعریف شده است
که در آن  و
و  پتانسیل های فاز رسانای الکترون (یکی برای هر الکترود)، E pos و E neg پتانسیل های الکترود هستند و
پتانسیل های فاز رسانای الکترون (یکی برای هر الکترود)، E pos و E neg پتانسیل های الکترود هستند و  افت پتانسیل روی فاز الکترولیت جداکننده الکترودها است.
افت پتانسیل روی فاز الکترولیت جداکننده الکترودها است.
چگالی جریان سلول باتری، سلول i (واحد SI: A·m − 2 )، به صورت تعریف می شود
که در آن R sol (واحد SI: Ω · m 2 ) مقاومت محلول است.
برای فرمول جهانی، افت پتانسیل در فاز محلول الکترولیت توسط رابطه به دست می آید
که در آن A sep (واحد SI: m2 ) سطح مقطع جداکننده و سلول I (واحد SI: A) جریان سلول باتری است.
برای فرمولاسیون محلی از رابطه زیر استفاده می شود
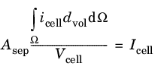
که در آن سلول V حجم سلول و Ω دامنه انتخابی است که در آن رابط تک ذره فعال است. توجه داشته باشید که d vol سطح مقطع سلول در 1D، ضخامت خارج از صفحه در 2D و 1D با تقارن محوری، و برابر با 1 در 3D و 2D با ابعاد فضای تقارن محوری است. در یک بعدی با تقارن محوری و دو بعدی با تقارن محوری، عبارات محاسبهکننده انتگرالهای حجمی نیز در 2 πr ضرب میشوند .
اگر ضخامت جداکننده L sep و کسر حجمی ε sep اشغال شده توسط جداکننده در باتری مشخص باشد، میتوان ناحیه جداکننده A sep را از رابطه زیر محاسبه کرد.
مقاومت محلول در جداکننده R sol,sep را می توان از ضخامت جداکننده و هدایت الکترولیت موثر σl , eff (تصحیح تخلخل جداکننده را محاسبه می کند) به شرح زیر محاسبه می شود.
برای جبران سهم مقاومت اهمی ناشی از افت پتانسیل الکترولیت در الکترودها، موارد فوق را نیز می توان در کسری عدد X ، معمولاً بزرگتر از 1 ضرب کرد.
تعادل بار برای هر الکترود برای حالت کلی به شرح زیر است:
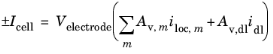
که در آن الکترود V حجم الکترود متخلخل است، i loc چگالی جریان میانافزایی محلی، i dl چگالی جریان دو لایه است و A v نشاندهنده سطح ویژه فعال است.
برای فرمول محلی، تراز شارژ به صورت زیر ارائه می شود:
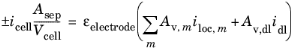
که در آن الکترود ε کسر حجمی الکترود متخلخل در باتری است.
در معادلات بالا علامت + برای الکترود مثبت و علامت – برای الکترود منفی اعمال می شود. در این رابط، جریان های شارژ مثبت و جریان های تخلیه منفی هستند.
انتشار در ذرات ماده فعال در الکترودهای مثبت و منفی توسط قانون دوم فیک به شرح زیر است.
که در آن cs غلظت گونه های درون گیر در فاز جامد و Ds ضریب انتشار فاز جامد است . معادله انتشار به صورت سراسری یا محلی (به ترتیب بسته به انتخاب فرمول جهانی یا محلی) توسط این رابط فیزیک در یک بعد شبه اضافی 1 بعدی مطابق با بعد ذره حل می شود. گرادیان در مختصات دکارتی، استوانهای یا کروی محاسبه میشود، بسته به این که ذرات بهترتیب بهعنوان پولک، میله یا کره توصیف شوند.
شرایط مرزی در مرکز و سطح ذره به شرح زیر است:
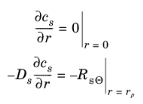
که در آن r p شعاع ذره ماده فعال الکترود است و Rs Θ نشان دهنده شار مولی کاتیون در سطح ذره است که در اثر واکنش های درج الکتروشیمیایی ایجاد می شود .
در سطح ذرات جامد، شار مولی با سرعت واکنش میانافزایی لیتیوم جفت میشود و معادله زیر اعمال میشود:
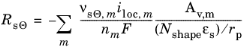
که در آن آخرین فاکتور (معمولاً برابر با 1) یک ضریب پوسته پوسته شدن است که تفاوتهای بین سطح ( Av ,m ) مورد استفاده برای محاسبه چگالی جریان حجمی و مساحت سطح ذرات در مدل انتشار لیتیوم جامد را محاسبه میکند. ν s Θ نشان دهنده ضریب استوکیومتری گونه های درونگیر در ذرات الکترود است، n m تعداد الکترون های منتقل شده و ε s کسر حجمی فاز الکترود در الکترود متخلخل است. شکل N برای مختصات دکارتی 1، برای استوانه ای 2 و برای مختصات کروی 3 است.
اگر ضریب انتشار فاز جامد بسیار بزرگ باشد و/یا اگر شیب غلظت مکانی در ذره را بتوان نادیده گرفت، تکامل غلظت فاز جامد در زمان را می توان از
منبع مولی Rs Θ در الکترودهای مثبت و منفی به صورت زیر داده می شود :
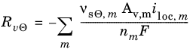
حجم سلول باتری، ظرفیت میزبان الکترود و کسر حجمی
در 0D سلول V حجم سلول باتری توسط کاربر مشخص می شود. در ابعاد بالاتر، سلول V حجم سلول بر اساس تعریف می شود
که در آن Ω دامنه انتخابی است که در آن رابط تک ذره فعال است، و d vol سطح مقطع سلول در 1D، ضخامت خارج از صفحه در 2D و 1D با تقارن محوری است و برابر با 1 در 3D است. و دو بعدی با ابعاد فضایی تقارن محوری. در یک بعدی با تقارن محوری و دو بعدی با تقارن محوری، عبارات محاسبهکننده انتگرالهای حجمی نیز در 2 πr ضرب میشوند . توجه داشته باشید که برای برخی موارد، سلول V به صراحت فقط برای محاسبه متغیرهای منبع گرما مورد نیاز است.
الکترود V حجم الکترود متخلخل با توجه به حجم سلول مرتبط است
ظرفیت میزبان الکترود به کسر حجمی الکترود مربوط می شود. برای فرمول جهانی، رابطه زیر برای مقدار میزبان Q ماده میزبان فعال ( واحد SI: C) برقرار است:
در جایی که Δ soc پنجره حالت شارژ مجاز ماده الکترود است و c s، max حداکثر غلظت گونه های درونگیر است.
برای فرمول محلی، رابطه زیر اعمال می شود:
در این رابط، ظرفیت های میزبان الکترود را می توان با ارائه مقدار مواد قابل چرخش (ظرفیت سلول) و یک رابطه متعادل کننده بین دو الکترود، یا با ارائه صریح بخش های حجمی الکترود در سلول مشخص کرد. فرض می شود که مقدار گونه های چرخه پذیر از مواد الکترود مثبت منشاء می گیرد. در برخی از شیمی باتری ها، به عنوان مثال باتری های لیتیوم یون، مقدار ماده میزبان در هر دو الکترود منحرف می شود. به عنوان مثال، باتری های لیتیوم یونی الکترودهای مبتنی بر کربن منفی اغلب در مقایسه با الکترود مثبت بیش از حد استفاده می شوند تا از آبکاری فلز لیتیوم در طول شارژ با سرعت بالا جلوگیری شود. گونه های چرخه پذیر در برخی موارد می توانند به طور مستقیم در اولین چرخه های “تشکیل” پس از مونتاژ سلولی به دلیل واکنش های انگلی از بین بروند. یک مثال معمولی تشکیل لایه SEI بر روی ذرات گرافیت منفی در باتری های لیتیوم یونی است. بنابراین روابط زیر اعمال می شود:
که در آن f cycl، از دست دادن کسری گونه های چرخه پذیر، و f میزبان، منفی، بیش از کسری از مواد میزبان فعال منفی را از دست می دهد.
توزیع اولیه شارژ در سلول باتری
وضعیت اولیه شارژ باتری به صراحت توسط مقادیر غلظت اولیه گونه های فعال در هر الکترود تعیین می شود. با این حال، این سطوح غلظت همیشه از پیش مشخص نیست. یک مرحله مطالعه اولیه توزیع جریان ممکن است برای محاسبه سطوح غلظت اولیه دو الکترود بر اساس ورودی در بخش توزیع بار اولیه استفاده شود. وضعیت شارژ اولیه سلول، ولتاژ سلول یا وضعیت شارژ الکترود (انفرادی) را می توان مشخص کرد.
ظرفیت سلول باتری، سلول Q ، 0 (واحد SI: C)، برابر است با مجموع بار گونه های قابل چرخش، سیکل Q ، در الکترودهای مثبت و منفی.
سیکل Q شارژ گونه قابل چرخش در یک الکترود برای فرمول جهانی به صورت زیر تعریف می شود:
که در آن cs ,avg میانگین غلظت گونه است که در ابتدا، زمانی که هیچ گرادیان غلظتی در ذرات الکترود وجود ندارد، برابر با غلظت در سطح ذرات الکترود، cs , surf است . soc min حداقل میزان بار مجاز در مواد الکترود است.
برای فرمول محلی، رابطه زیر برقرار است:
در صورتی که ورودی کاربر سلول سوسیال حالت شارژ اولیه سلول، 0 باشد ، مقدار چرخهپذیر گونهها در هر الکترود به ظرفیت سلول به شرح زیر مربوط میشود:
حالت شارژ سلول بین 0 تا 1 است. حالت شارژ 0 نشان می دهد که سلول کاملاً تخلیه شده است و اگر 1 باشد سلول کاملاً شارژ شده است.
در صورتی که ورودی کاربر ولتاژ سلول اولیه E سلول، 0 باشد ، رابطه زیر برای فرمول جهانی اعمال می شود.
برای فرمول محلی، رابطه زیر برقرار است:
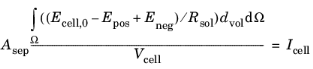
اگر حالت شارژ اولیه عملیاتی الکترود (soc op,pos,0 و soc op,neg,0 ) مشخص شود، روابط زیر اعمال میشود:
منابع حرارتی الکتروشیمیایی
برای مدلسازی تعادل انرژی یک سلول الکتروشیمیایی، از رابط انتقال حرارت برای مدلسازی انتقال گرما و رابط باتری تک ذره برای تولید منابع گرما و سینکهای ناشی از جریانهای الکتروشیمیایی استفاده میشود.
عبارات منابع گرما در الکترود متخلخل منفی/مثبت (به دلیل واکنش الکتروشیمیایی) الکترود Qh ، (واحد SI: W/m 3 ) به شرح زیر است:
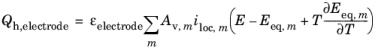
گرمایش اهمی در فاز الکترولیت Qh ,sol (واحد SI: W/m 3 ) است
کل منبع گرمای سلول حجمی Qh ، سلول (واحد SI: W/m 3 ) را می توان به صورت نوشتاری




