باتری نارنجی
معرفی
این مدل آموزشی به عنوان مقدمه ای بر مدل سازی الکتروشیمی در COMSOL Multiphysics عمل می کند. این مثال جریان و غلظت یون های فلزی محلول را در یک باتری (سلول خوردگی) ساخته شده از یک نارنجی و دو میخ فلزی شبیه سازی می کند.
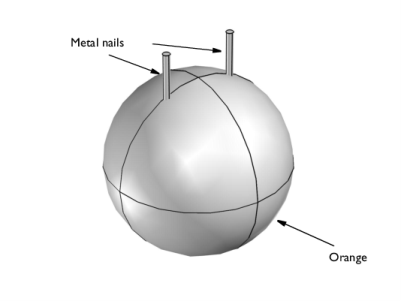
شکل 1: هندسه مدل شده. نارنجی و دو میخ فلزی. (به دلیل رسانایی بالای میخ های فلزی، فقط خمیر نارنجی رنگ در حوزه محاسباتی قرار می گیرد.)
این نوع باتری معمولا در نمایش های کلاس شیمی استفاده می شود. به جای پرتقال می توان از لیمو یا سیب زمینی نیز استفاده کرد.
تعریف مدل
اسید سیتریک و یون های مختلف دیگر در پرتقال به عنوان الکترولیت عمل می کنند و استفاده از میخ های فلزات مختلف به عنوان الکترود، پتانسیل گالوانیکی را روی سلول ایجاد می کند.
در این مثال، یک میخ روی به عنوان یکی از الکترودها استفاده می شود که باعث واکنش الکترود زیر می شود:
میخ دیگر از مس تشکیل شده است و در اینجا تکامل هیدروژن فرض می شود:
Eq ,0 در بالا نشان دهنده پتانسیل تعادل در شرایط استاندارد در مقابل یک الکترود هیدروژن استاندارد (SHE) است. در مدل، پتانسیل تعادل برای pH و غلظت روی خمیر پرتقال با استفاده از معادله نرنست تصحیح می شود.
مدل برای جریان در نارنجی و الکترودها با استفاده از رابط توزیع جریان ثانویه تنظیم شده است. بنابراین جریان الکترولیت در رنگ نارنجی با قانون اهم حل می شود. رسانایی میخ های فلزی آنقدر زیاد است که حوزه های الکترود در مدل گنجانده نشده است، در عوض از شرایط مرزی روی سطوح میخ برای تنظیم پتانسیل میخ استفاده می شود. یک میخ به زمین متصل می شود و دیگری روی یک پتانسیل سلولی تنظیم می شود تا با شرایط فعلی کامل مطابقت داشته باشد. این با وضعیتی مطابقت دارد که در آن سلول از نظر گالوانوستاتیک کنترل می شود، به عنوان مثال، با استفاده از یک پتانسیواستات.
عبارات نوع باتلر-ولمر، با چگالی جریان مبادله وابسته به غلظت برای واکنش روی، برای سینتیک الکترود روی سطح میخ ها در رنگ نارنجی استفاده می شود.
مقادیر اولیه پتانسیل الکترولیت مطابق با پتانسیل یک سلول در مدار باز است (یعنی بدون پتانسیل فعال سازی). طبق تعریف مازاد پتانسیل:
مقدار اولیه می شود:
در توسعه مدل، انتقال یونهای روی محلول در رنگ نارنجی از واکنش الکترود روی توسط رابط حمل و نقل گونههای رقیق شده در یک شبیهسازی وابسته به زمان مدلسازی میشود. این فرض می کند که انتقال یون روی را می توان با انتشار طبق قانون فیک توصیف کرد. علاوه بر این، سینتیک الکترود روی برای وابسته بودن به غلظت روی اصلاح می شود که با حل شدن بیشتر و بیشتر روی در رنگ نارنجی افزایش می یابد.
جریان سلول روی مقدار ثابت 1 میلی آمپر و غلظت روی روی 0.001 mol/m3 در شروع شبیه سازی تنظیم می شود. تمام مرزها به جز الکترود روی عایق هستند.
نتایج و بحث
شکل 2 میدان پتانسیل را در رنگ نارنجی نشان می دهد. با عبور جریان از الکترود روی (چپ) به الکترود بالایی (راست) پتانسیل کاهش می یابد. بخش اصلی افت ولتاژ سلول به دلیل تلفات اهمی در الکترولیت است.
عملکرد باتری را احتمالاً می توان با استفاده از الکترولیت با رسانایی بالاتر (مثلاً یک لیمو به جای پرتقال) یا با کاهش فاصله بین ناخن ها افزایش داد.
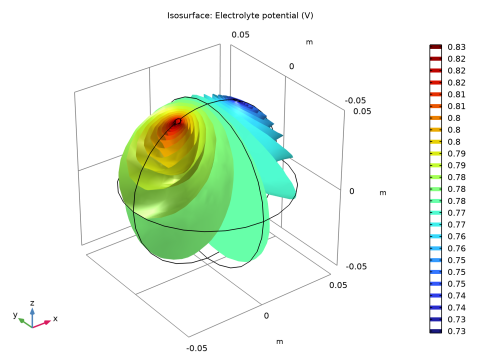
شکل 2: میدان پتانسیل در الکترولیت در t = 0.
شکل 3 نمودار پلاریزاسیون را با افزایش جریان کل باتری از 0 به 1 میلی آمپر نشان می دهد. تغییر بزرگ در ولتاژ سلول که در جریان های کم مشاهده می شود به دلیل تلفات بیش از حد پتانسیل در الکترود روی است. افزایش مساحت الکترود روی این اثر را کاهش می دهد.
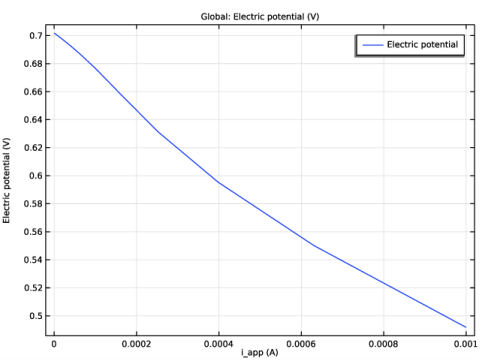
شکل 3: نمودار پلاریزاسیون برای غلظت های اولیه.
شکل 4 سطح غلظت 0.2 mol/m3 یون روی را پس از کارکردن باتری به مدت پنج دقیقهنشان می دهدشکل 5 نشان می دهد که سطح هم سطح 0.2 mol/m3 پس از یک ساعت تا چه حدرسیده است.
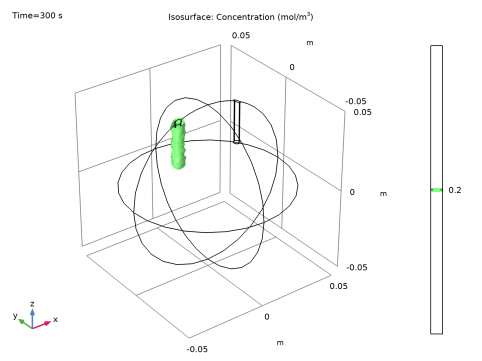
شکل 4: 0.2 mol/m3 غلظت روی هم سطح بعد از پنج دقیقه.

شکل 5: 0.2 mol/m3 غلظت روی هم سطحی پس از یک ساعت.
شکل 6 نشان می دهد که چگونه پتانسیل سلول با زمان تکامل می یابد. به دلیل افزایش یون روی در الکترود میخ روی، پتانسیل سلول باتری برای جریان ثابت سلول کاهش می یابد.
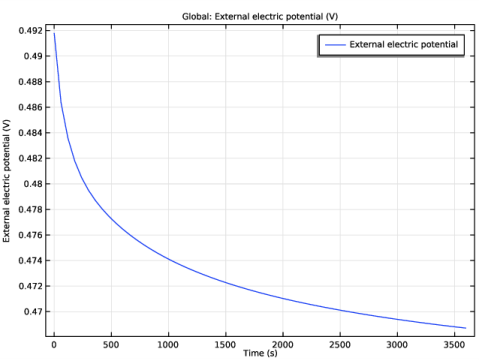
شکل 6: پتانسیل سلول در برابر زمان.
تمرینات و برنامه های افزودنی پیشنهادی مدل
شعاع میخ ها و مقدار رسانایی الکترولیت را تغییر دهید و بررسی کنید که چگونه این موضوع بر نمودار پلاریزاسیون تأثیر می گذارد.
غلظت هیدروژن در مدل گنجانده نشده است. برای نظارت بر تغییر pH سلول، یک غلظت اضافی را به گره متغیرهای وابسته در انتقال گونههای رقیق اضافه کنید، سپس با استفاده از یک گره اتصال سطحی الکترود، شار یونهای هیدروژن را روی سطح مس جفت کنید.
یونهای روی محلول ممکن است لایهای از هیدروکسید روی را روی سطح روی تشکیل دهند که منجر به افت پتانسیل اضافی میشود. می توانید از بخش مقاومت فیلم در گره سطح الکترود برای درج این افت احتمالی استفاده کنید. به عنوان مثال، مقدار مقاومت فیلم می تواند تابعی از متغیر غلظت یون روی در خمیر کاغذ باشد. از طرف دیگر، میتوانید یک رابط Surface Reactions برای مدلسازی تجمع غلظت سطحی هیدروکسید روی اضافه کنید و سپس مقاومت فیلم را با غلظت هیدروکسید ترکیب کنید.
مسیر کتابخانه برنامه: Electrochemistry_Module/Tutorials /orange_battery
دستورالعمل های مدل سازی
از منوی File ، New را انتخاب کنید .
جدید
در پنجره جدید ، روی  Model Wizard کلیک کنید .
Model Wizard کلیک کنید .
مدل جادوگر
1 | در پنجره Model Wizard ، روی |
2 | در درخت Select Physics ، Electrochemistry>Primary and Secondary Current Distribution>Secondary Current Distribution (cd) را انتخاب کنید . |
3 | روی افزودن کلیک کنید . |
4 |
5 | در درخت انتخاب مطالعه ، General Studies>Stationary را انتخاب کنید . |
6 |
هندسه 1
با ترسیم هندسه شروع کنید. یک کره (نارنجی) و دو استوانه (میخ های فلزی).
کره 1 (sph1)
1 | در نوار ابزار Geometry ، روی |
2 | در پنجره تنظیمات برای Sphere ، بخش Size را پیدا کنید . |
3 | در قسمت متن Radius ، 5e-2 را تایپ کنید . |
ناخن روی
1 | در نوار ابزار Geometry ، روی |
2 | در پنجره تنظیمات سیلندر ، روی میخ Zinc را در قسمت نوشتار برچسب تایپ کنید . |
3 | قسمت Size and Shape را پیدا کنید . در قسمت متن Radius ، 2e-3 را تایپ کنید . |
4 | در قسمت متن ارتفاع ، 5e-2 را تایپ کنید . |
5 | قسمت Position را پیدا کنید . در قسمت متن x ، -2e-2 را تایپ کنید . |
6 | در قسمت متن z ، 2e-2 را تایپ کنید . |
با فعال کردن Resulting Objects Selection میتوانید به راحتی تمام مرزهای میخ را بعداً هنگام تنظیم فیزیک انتخاب کنید.
7 | قسمت Selections of Resulting Entities را پیدا کنید . تیک گزینه Resulting objects selection را انتخاب کنید . |
8 | از فهرست نمایش در فیزیک ، همه سطوح را انتخاب کنید . |
میخ مسی
استوانه را کپی کنید و موقعیت x را تغییر دهید تا میخ دوم بکشید.
1 | روی Zinc nail کلیک راست کرده و Duplicate را انتخاب کنید . |
2 | در پنجره تنظیمات سیلندر ، Copper nail را در قسمت نوشتار برچسب تایپ کنید . |
3 | قسمت Position را پیدا کنید . در قسمت متن x ، 2e-2 را تایپ کنید . |
تعاریف جهانی
برخی از پارامترهای جهانی را از یک فایل بارگیری کنید. اینها در چندین مکان در مدل استفاده خواهند شد.
پارامترهای 1
1 | در پنجره Model Builder ، در قسمت Global Definitions روی Parameters 1 کلیک کنید . |
2 | در پنجره تنظیمات برای پارامترها ، بخش پارامترها را پیدا کنید . |
3 |
4 | به پوشه Application Libraries مدل بروید و روی فایل orange_battery_parameters.txt دوبار کلیک کنید . |
تعاریف
همچنین برخی از تعاریف متغیر را از یک فایل بارگیری کنید.
متغیرهای 1
1 | در پنجره Model Builder ، در قسمت Component 1 (comp1) روی Definitions کلیک راست کرده و Variables را انتخاب کنید . |
2 | در پنجره تنظیمات برای متغیرها ، بخش متغیرها را پیدا کنید . |
3 |
4 | به پوشه Application Libraries مدل بروید و روی فایل orange_battery_variables.txt دوبار کلیک کنید . |
توزیع جریان ثانویه (CD)
اکنون، شروع به تنظیم مدل توزیع فعلی کنید.
انتخاب کل رابط فیزیک را فقط به دامنه نارنجی تغییر دهید.
1 | در پنجره Model Builder ، در قسمت Component 1 (comp1) بر روی Secondary Current Distribution (cd) کلیک کنید . |
2 | فقط دامنه 1 را انتخاب کنید. |
همچنین یک انتخاب برای دامنه نارنجی ایجاد کنید. اگر هندسه نیاز به تغییر در آینده داشته باشد، این امر تسهیل خواهد شد. انتخاب ها به طور کلی روشی مناسب برای گروه بندی قسمت های مختلف هندسه با هم هستند.
3 | در پنجره تنظیمات برای توزیع جریان ثانویه ، قسمت انتخاب دامنه را پیدا کنید . |
4 |
5 | در کادر محاوره ای Create Selection ، در قسمت متن انتخاب نام ، نارنجی را تایپ کنید . |
6 | روی OK کلیک کنید . |
الکترولیت 1
قبلاً یک گره Electrolyte به صورت پیش فرض به مدل اضافه شده است. انتخاب روی تمام دامنههای انتخابی رابط فیزیک قفل میشود، که در این مورد فقط نارنجی است. هدایت الکترولیت را تنظیم کنید.
1 | در پنجره Model Builder ، در قسمت Component 1 (comp1)> Secondary Current Distribution (cd) روی Electrolyte 1 کلیک کنید . |
2 | در پنجره تنظیمات الکترولیت ، بخش الکترولیت را پیدا کنید . |
3 | از لیست σ l ، User defined را انتخاب کنید . در قسمت متن مرتبط، سیگما را تایپ کنید . |
سطح الکترود 1
از گره های سطح الکترود برای تعریف پتانسیل الکترود فلزی و رابط الکترود-الکترولیت استفاده کنید. از عبارت Butler-Volmer برای الکترود روی استفاده کنید. سینتیک هیدروژن بسیار سریع فرض می شود به طوری که یک بیان خطی شده باتلر-ولمر قابل استفاده است.
1 | در نوار ابزار Physics ، روی |
2 | در پنجره تنظیمات برای سطح الکترود ، بخش انتخاب مرز را پیدا کنید . |
3 | از لیست انتخاب ، ناخن روی را انتخاب کنید . |
شفافیت را فعال کنید و مرزهای فعال را در پنجره گرافیکی بررسی کنید.
4 |
واکنش الکترود 1
1 | در پنجره Model Builder ، روی Electrode Reaction 1 کلیک کنید . |
2 | در پنجره تنظیمات برای واکنش الکترود ، بخش پتانسیل تعادل را پیدا کنید . |
3 | از لیست Eq ، معادله Nernst را انتخاب کنید . |
4 | در قسمت متن Eq ,ref ( T ) Eeqref_Zn را تایپ کنید . |
5 | در قسمت متن C O ، c_Zn2/c_ref را تایپ کنید . |
6 | قسمت ضرایب استوکیومتری را پیدا کنید . در قسمت متن n ، 2 را تایپ کنید . |
7 | بخش سینتیک الکترود را پیدا کنید . از لیست نوع عبارت Kinetics ، Butler-Volmer را انتخاب کنید . |
8 | از لیست نوع چگالی جریان Exchange ، From Nernst Equation را انتخاب کنید . |
9 | در قسمت متن i 0,ref ( T ) i0ref_Zn را تایپ کنید . |
10 | در قسمت متن α a ، alpha_a_Zn را تایپ کنید . |
سطح الکترود 2
اکنون الکترود مس را به روشی مشابه تعریف کنید. ابتدا یک پارامتر برای جریان کل اضافه کنید. این پارامتر همچنین در مطالعه برای انجام یک جاروب پلاریزاسیون گالوانیکی بر روی سلول استفاده خواهد شد.
1 | در نوار ابزار Physics ، روی |
2 | در پنجره تنظیمات برای سطح الکترود ، بخش انتخاب مرز را پیدا کنید . |
3 | از لیست انتخاب ، میخ مسی را انتخاب کنید . |
4 | بخش وضعیت پتانسیل فاز الکترود را پیدا کنید . از لیست شرایط پتانسیل فاز الکترود ، جریان کل را انتخاب کنید . |
5 | در قسمت I l,total text، -i_app را تایپ کنید . |
واکنش الکترود 1
1 | در پنجره Model Builder ، روی Electrode Reaction 1 کلیک کنید . |
2 | در پنجره تنظیمات برای واکنش الکترود ، بخش پتانسیل تعادل را پیدا کنید . |
3 | از لیست Eq ، معادله Nernst را انتخاب کنید . |
4 | در قسمت متن C O ، c_H0/c_ref را تایپ کنید . |
5 | بخش سینتیک الکترود را پیدا کنید . در قسمت متن i 0 ، i0_H2 را تایپ کنید . |
مقادیر اولیه 1
ما از سینتیک غیرخطی در مدل استفاده می کنیم. یک مقدار اولیه برای پتانسیل الکترولیت به منظور کاهش زمان حل کننده و بهبود همگرایی ارائه دهید. به عنوان یک قاعده کلی، اغلب می توان از منفی پتانسیل تعادل الکترود زمین شده به عنوان مقدار اولیه پتانسیل الکترولیت استفاده کرد.
1 | در پنجره Model Builder ، در قسمت Component 1 (comp1)>Secondary Current Distribution (cd) روی مقادیر اولیه 1 کلیک کنید . |
2 | در پنجره تنظیمات برای مقادیر اولیه ، قسمت مقادیر اولیه را پیدا کنید . |
3 | در قسمت فیل متن، -E_eq_Zn0 را تایپ کنید . |
تعاریف جهانی
ورودی های مدل پیش فرض
مقدار دمای مورد استفاده در کل مدل را تنظیم کنید.
1 | در پنجره Model Builder ، در قسمت Global Definitions، روی Default Model Inputs کلیک کنید . |
2 | در پنجره تنظیمات برای ورودی های مدل پیش فرض ، بخش Browse Model Inputs را پیدا کنید . |
3 | در درخت، General>Temperature (K) – minput.T را انتخاب کنید . |
4 | زیربخش عبارت برای انتخاب باقیمانده را پیدا کنید . در قسمت متن دما ، T را تایپ کنید . |
مطالعه 1
از آنجایی که ما از تنظیمات مش پیش فرض استفاده می کنیم، مدل اکنون برای حل آماده است.
1 | در نوار ابزار صفحه اصلی ، |
نتایج
پتانسیل الکترولیت (cd)
نمودارهای پتانسیل های الکترولیت به طور پیش فرض ایجاد می شوند.
برای تجسم میدان پتانسیل در الکترولیت از یک سطح همسان استفاده کنید.
ایزورفیس بالقوه
1 | در نوار ابزار صفحه اصلی ، روی |
2 | در پنجره تنظیمات برای گروه طرح سه بعدی ، Potential Isosurface را در قسمت نوشتار Label تایپ کنید . |
ایزورفیس 1
1 | روی Potential Isosurface کلیک راست کرده و Isosurface را انتخاب کنید . |
2 | در پنجره تنظیمات برای Isosurface ، بخش Levels را پیدا کنید . |
3 | در فیلد متنی مجموع سطوح ، 25 را تایپ کنید . |
4 | در نوار ابزار Potential Isosurface ، روی |
5 |
6 |
با شکل 2 در بخش نتایج و بحث مقایسه کنید.
مطالعه 1
مرحله 1: ثابت
اکنون از یک جارو کمکی برای حل طیف وسیعی از جریان های سلولی به منظور ایجاد نمودار قطبی استفاده کنید.
1 | در پنجره Model Builder ، در بخش مطالعه 1 ، روی Step 1: Stationary کلیک کنید . |
2 | در پنجره تنظیمات برای Stationary ، برای گسترش بخش Study Extensions کلیک کنید . |
3 | کادر بررسی جارو کمکی را انتخاب کنید . |
4 |
5 | در جدول تنظیمات زیر را وارد کنید: |
نام پارامتر | لیست مقادیر پارامتر | واحد پارامتر |
i_app (جریان کاربردی) | محدوده 0 10(-5،0.2،-3) | آ |
6 | در نوار ابزار صفحه اصلی ، |
نتایج
نمودار پلاریزاسیون را به صورت زیر ایجاد کنید:
طرح پلاریزاسیون
1 | در نوار ابزار صفحه اصلی ، روی |
2 | در پنجره تنظیمات برای گروه طرح 1 بعدی ، پلاریزاسیون پلات را در قسمت نوشتار برچسب تایپ کنید . |
جهانی 1
1 | روی پلاریزاسیون Plot کلیک راست کرده و Global را انتخاب کنید . |
2 | در پنجره تنظیمات برای جهانی ، روی Replace Expression در گوشه سمت راست بالای بخش y-Axis Data کلیک کنید . از منو، Component 1 (comp1)>Secondary Current Distribution>cd.phis_es2 – Electric Potential – V را انتخاب کنید . |
3 | در نوار ابزار Polarization Plot ، روی |
با شکل 3 در بخش نتایج و بحث مقایسه کنید.
جزء 1 (COMP1)
اکنون، مدل را گسترش دهید تا ولتاژ باتری در طول زمان در جریان بار مشخص بررسی شود. با افزودن یک رابط فیزیک برای مدیریت حمل و نقل جرم یونهای روی شروع کنید.
فیزیک را اضافه کنید
1 | در نوار ابزار Home ، روی |
2 | به پنجره Add Physics بروید . |
3 | در درخت، Chemical Species Transport>Transport of Diluted Species (tds) را انتخاب کنید . |
4 | روی Add to Component 1 در نوار ابزار پنجره کلیک کنید . |
5 | در نوار ابزار Home ، روی |
حمل و نقل گونه های رقیق شده (TDS)
1 | در پنجره تنظیمات برای حمل و نقل گونه های رقیق ، قسمت انتخاب دامنه را پیدا کنید . |
2 | از لیست انتخاب ، نارنجی را انتخاب کنید . |
پالپ نارنجی ساکن است، بنابراین می توان همرفت را در مدل نادیده گرفت.
3 | بخش مکانیزم های حمل و نقل را پیدا کنید . چک باکس Convection را پاک کنید . |
(به دلیل وجود تعداد زیادی یون دیگر در خمیر کاغذ که به عنوان الکترولیت پشتیبان عمل می کنند، گرادیان های پتانسیل را کوچک فرض می کنیم و از این رو تأثیر انتقال مهاجرت یون های روی را نادیده می گیریم.)
کوپلینگ سطح الکترود 1
برای این مثال، از مقدار ضریب انتشار پیشفرض در گره ویژگیهای Transport استفاده میکنیم، بنابراین هیچ تنظیماتی در گره دامنه پیشفرض مورد نیاز نیست. مراحل زیر جریان های واکنش الکتروشیمیایی را به شار یونی در سطح الکترود متصل می کند:
1 | روی Component 1 (comp1)>Transport of Diluted Species (tds) کلیک راست کرده و Surface Reactions>Electrode Surface Coupling را انتخاب کنید . |
2 |
3 | در پنجره تنظیمات برای اتصال سطح الکترود ، بخش انتخاب مرز را پیدا کنید . |
4 | از لیست انتخاب ، ناخن روی را انتخاب کنید . |
ضرایب واکنش 1
1 | در پنجره Model Builder ، گره Electrode Surface Coupling 1 را گسترش دهید ، سپس روی Reaction Coefficients 1 کلیک کنید . |
2 | در پنجره تنظیمات برای ضرایب واکنش ، بخش ورودی مدل را پیدا کنید . |
3 | از لیست i loc ، چگالی جریان محلی ، واکنش الکترود 1 (cd/es1/er1) را انتخاب کنید . |
4 | قسمت ضرایب استوکیومتری را پیدا کنید . در قسمت متن n ، 2 را تایپ کنید . |
5 | در قسمت متن ν c ، -1 را تایپ کنید . |
عدد استوکیومتری به عدد استوکیومتری گونههای واکنشدهنده اشاره دارد که به عنوان یک واکنش کاهشی نوشته میشود.
مقادیر اولیه 1
غلظت اولیه یون روی را در شروع شبیه سازی وابسته به زمان تنظیم کنید.
1 | در پنجره Model Builder ، در قسمت Component 1 (comp1)>Transport of Diluted Species (tds) روی مقادیر اولیه 1 کلیک کنید . |
2 | در پنجره تنظیمات برای مقادیر اولیه ، قسمت مقادیر اولیه را پیدا کنید . |
3 | در قسمت متن c ، c_Zn20 را تایپ کنید . |
تعاریف
غلظت یون روی دیگر ثابت نیست. متغیر غلظت یون روی را تغییر دهید تا به غلظت محلی وابسته باشد. نام این متغیر به طور پیش فرض c در رابط Transport of Diluted Species است.
متغیرهای 1
1 | در پنجره Model Builder ، در قسمت Component 1 (comp1)>Definitions روی Variables 1 کلیک کنید . |
2 | در پنجره تنظیمات برای متغیرها ، بخش متغیرها را پیدا کنید . |
3 | در جدول تنظیمات زیر را وارد کنید: |
نام | اصطلاح | واحد | شرح |
c_Zn2 | ج | mol/m³ | غلظت یون روی (استفاده شده در عبارات بالا) |
ریشه
یک مطالعه جدید وابسته به زمان برای شبیه سازی غلظت ایجاد کنید.
اضافه کردن مطالعه
1 | در نوار ابزار Home ، روی |
2 | به پنجره Add Study بروید . |
3 | زیربخش مطالعات را پیدا کنید . در درخت انتخاب مطالعه ، مطالعات از پیش تعیین شده برای واسط های فیزیک انتخاب شده > توزیع جریان ثانویه > وابسته به زمان با مقداردهی اولیه را انتخاب کنید . |
4 | روی Add Study در نوار ابزار پنجره کلیک کنید . |
5 | در نوار ابزار Home ، روی |
مطالعه 2
مرحله 1: راه اندازی توزیع فعلی
از توزیع جریان ثانویه در مرحله اولیه سازی استفاده کنید.
1 | در پنجره تنظیمات برای راهاندازی توزیع فعلی ، بخش تنظیمات مطالعه را پیدا کنید . |
2 | از لیست نوع توزیع فعلی ، ثانویه را انتخاب کنید . |
مرحله 2: وابسته به زمان
1 | در پنجره Model Builder ، روی Step 2: Time Dependent کلیک کنید . |
2 | در پنجره تنظیمات مربوط به زمان وابسته ، قسمت تنظیمات مطالعه را پیدا کنید . |
3 | در قسمت متنی زمان خروجی ، range(0,60,3600) را تایپ کنید . |
4 | در نوار ابزار صفحه اصلی ، |
نتایج
پتانسیل سلولی در مقابل زمان
نموداری برای چگونگی تغییر پتانسیل سلول با زمان به طور پیش فرض ایجاد می شود.
1 | در پنجره تنظیمات برای گروه طرح 1 بعدی ، Cell Potential vs. Time را در قسمت نوشتار برچسب تایپ کنید . |
2 | در نوار ابزار Cell Potential vs. Time ، روی |
با شکل 6 در بخش نتایج و بحث مقایسه کنید.
غلظت روی را در پرتقال به صورت زیر رسم کنید:
غلظت ایزورفیس
1 | در نوار ابزار صفحه اصلی ، روی |
2 | در پنجره تنظیمات برای گروه طرح سه بعدی ، Concentration Isosurface را در قسمت متن برچسب تایپ کنید . |
3 | قسمت Data را پیدا کنید . از لیست مجموعه داده ، مطالعه 2/راه حل 2 (sol2) را انتخاب کنید . |
4 | از لیست زمان (ها) ، 300 را انتخاب کنید . |
ایزورفیس 1
1 | روی Concentration Isosurface کلیک راست کرده و Isosurface را انتخاب کنید . |
2 | در پنجره تنظیمات برای Isosurface ، روی Replace Expression در گوشه سمت راست بالای بخش Expression کلیک کنید . از منو، Component 1 (comp1)>Transport of Diluted Species>Species c>c – Concentration – mol/m³ را انتخاب کنید . |
3 | قسمت Levels را پیدا کنید . از لیست روش ورود ، سطوح را انتخاب کنید . |
4 | در قسمت متن Levels 0.2 را تایپ کنید . |
5 | در نوار ابزار Concentration Isosurface ، روی |
6 |
7 |
با شکل 4 در بخش نتایج و بحث مقایسه کنید.
انیمیشن 1
مراحل زیر یک انیمیشن از سطح هم سطح یون روی در طول زمان شبیه سازی شده ایجاد می کند:
1 | در نوار ابزار نتایج ، روی |
2 | در پنجره تنظیمات برای انیمیشن ، بخش Target را پیدا کنید . |
3 | از لیست هدف ، Player را انتخاب کنید . |
4 | قسمت Scene را پیدا کنید . از لیست موضوع ، Concentration Isosurface را انتخاب کنید . |
5 | قسمت ویرایش انیمیشن را پیدا کنید . از لیست انتخاب زمان ، از لیست را انتخاب کنید . |
در t = 0 هیچ گرادیان غلظتی در رنگ نارنجی وجود ندارد. بنابراین، مرحله اول را پاک کنید.
6 | در لیست بارها ، 60 , 120 , 180 , 240 , 300 , 360 , 420 , 480 , 540 , 600 , 660 , 720 , 780 , 840 , 780 , 840 , 190 , 840 , 780 , 840 , 190 , 90 , 1320 , 1380 , 1440 , 1500 ,1560 ، 1620 ، 1680 ، 1740 ، 1800 ، 1860 ، 1920 ، 1980 ، 2040 ، 2100 ، 2160 ، 2220 ، 2280 ، 2220 ، 2520 ، 2580 ، 2640 ، 2700 ، 2760 ، 2820 ، 2880 ، 2940 ، 3000 ، 3000 ، _ _ 3060 ، 3120, 3180 , 3240 , 3300 , 3360 , 3420 , 3480 , 3540 و 3600 . |
7 |
8 |
آخرین فریم را در زمان 3600 ثانیه با شکل 5 در بخش نتایج و بحث مقایسه کنید.
مطالعه 1
مرحله 1: ثابت
توجه داشته باشید که اگر می خواهید مدل را با تغییر مقادیر پارامتر آزمایش کنید و نمودارهای قطبش جدید را با استفاده از مطالعه اول (ایستا) شبیه سازی کنید، باید رابط حمل و نقل گونه های رقیق شده را در آن مطالعه به صورت زیر غیرفعال کنید:
1 | در پنجره Model Builder ، در بخش مطالعه 1 ، روی Step 1: Stationary کلیک کنید . |
2 | در پنجره تنظیمات برای Stationary ، بخش Physics and Variables Selection را پیدا کنید . |
3 | در جدول تنظیمات زیر را وارد کنید: |
رابط فیزیک | حل کنید برای | فرم معادله |
توزیع جریان ثانویه (cd) | √ | اتوماتیک (ایستا) |
حمل و نقل گونه های رقیق شده (tds) | اتوماتیک (ایستا) |




